![\includegraphics[width=.9\linewidth]{schema.eps}](img6.png)
Giuseppe Dalba
|
In questi appunti vogliamo dimostrare che il rendimento di una
macchina termica che lavori a contatto con infinite sorgenti fra
una temperatura massima
|
![\includegraphics[width=.9\linewidth]{schema.eps}](img6.png)
|
L'integrale di Clausius (ovvero l'integrale degli scambi di calore
divisi per la temperatura a cui avvengono) per il ciclo termodinamico
![]() , che è reversibile per ipotesi, è sicuramente nullo. Possiamo
dividere questo integrale in due parti,
, che è reversibile per ipotesi, è sicuramente nullo. Possiamo
dividere questo integrale in due parti, ![]() e
e ![]() , nelle quali
rispettivamente si assorbe o si cede solo calore:
, nelle quali
rispettivamente si assorbe o si cede solo calore:
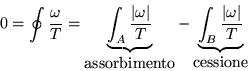
Possiamo minorare il primo integrale sostituendo
![]() al posto
della temperatura a cui lo scambio di calore avviene. Allo stesso
modo possiamo rimpiazzare
al posto
della temperatura a cui lo scambio di calore avviene. Allo stesso
modo possiamo rimpiazzare ![]() nel secondo integrale con
nel secondo integrale con
![]() ed
ottenere un valore più grande. A questo punto le temperature possono
essere portate fuori dal segno di integrazione, e
ed
ottenere un valore più grande. A questo punto le temperature possono
essere portate fuori dal segno di integrazione, e ![]() si
riduce semplicemente al calore assorbito
si
riduce semplicemente al calore assorbito
![]() o ceduto
o ceduto
![]() .
Siccome il secondo integrale ha un segno negativo, in entrambi i casi
stiamo sottovalutando l'integrale di Clausius, quindi;
.
Siccome il secondo integrale ha un segno negativo, in entrambi i casi
stiamo sottovalutando l'integrale di Clausius, quindi;
Questa relazione ci permette immediatamente di ricavare una
disuguaglianza fra il rendimento del ciclo ![]() e quello della
corrispondente macchina di Carnot (che è
e quello della
corrispondente macchina di Carnot (che è
![]() ):
):
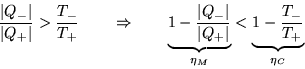
il che è equivalente a scrivere appunto
![]() , come
volevasi dimostrare. Quindi una macchina termica il cui fluido di
lavoro subisca un ciclo reversibile scambiando calore con infinite
sorgenti a temperatura compresa fra un valore minimo
, come
volevasi dimostrare. Quindi una macchina termica il cui fluido di
lavoro subisca un ciclo reversibile scambiando calore con infinite
sorgenti a temperatura compresa fra un valore minimo
![]() ed uno
massimo
ed uno
massimo
![]() ha rendimento inferiore alla machina di Carnot che
utilizza sorgenti fra le stesse temperature estreme.
Se la macchina termica
ha rendimento inferiore alla machina di Carnot che
utilizza sorgenti fra le stesse temperature estreme.
Se la macchina termica ![]() fosse una macchina reale, e pertanto
irreversibile, il suo rendimento sarebbe minore di quello della
corrispondente machina reversibile e quindi, a maggior ragione
sarebbe minore del rendimento della macchina di Carnot che
utilizza le sorgenti a temperatura
fosse una macchina reale, e pertanto
irreversibile, il suo rendimento sarebbe minore di quello della
corrispondente machina reversibile e quindi, a maggior ragione
sarebbe minore del rendimento della macchina di Carnot che
utilizza le sorgenti a temperatura
![]() e
e
![]() .
.