| Fig
1 |
Termoscopio fiorentino |
Temperatura ed equilibrio termico
Abbiamo accennato che
il principio zero consente di dare una definizione empirica della temperatura;
vediamo perché. Esso afferma che:
due
corpi in equilibrio termico con un terzo, sono in equilibrio termico tra loro.
In altre parole vige la proprietà transitiva:
se (A è in equilibrio con B) e ( B è in equilibrio con C) si ha anche che ( A è in equilibrio con C)
Un corpo a contatto con altri corpi si dice che č in equilibrio termico con essi
se nč si riscalda e né si raffredda (l’interazione si suppone avvenga solo
tra i corpi e non con l’ambiente).
La proprietŕ condivisa con i corpi
a contatto viene detta temperatura.
La temperatura rappresenta perciň la
misura del livello termico comune dei corpi a contatto.
| Fig
1 |
Termoscopio fiorentino |
Per rivelare la situazione di equilibrio uno dei tre corpi puň essere un termoscopio.
Per definire la temperatura occorre dotare il termoscopio di una scala. Si ottiene cosě un termometro.
Definizione Operativa della Temperatura
La temperatura č quella proprietŕ di un sistema che si misura con un termometro. La definizione completa di temperatura richiede una descrizione dettagliata di come č fatto un del termometro e della sua scala.
|
|
La definizione operativa di temperatura si basa sull’uso di una proprietŕ di una sostanza sensibile alla temperatura e sulla definizione dell’unitŕ di temperatura.
Tra le proprietŕ sensibili alla Temperatura, dal punto di vista tecnico, si ricorre spesso a proprietŕ termoelastiche ed a proprietŕ elettriche della materia. Sono molto diffusi i termometri che si basano sulla dilatazione termica dei materiali.
L'unitŕ di misura viene stabilita assegnando un insieme appropriato di riferimenti numerici che costituiscono la scala della temperatura. Si definiscono cosě le scale empiriche e la scala assoluta della temperatura. Una scala empirica č quella Centesimale.
Sviluppo di una scala empirica di temperatura: Scala Centesimale
Proprietŕ:
Dilatazione termica di un termometro al mercurio. Sia l la lunghezza
del tratto di mercurio nel capillare di vetro
![]() equazione
termometrica; l grandezza termometrica
equazione
termometrica; l grandezza termometrica
| Esempi di equazioni termometriche: |
|
|
|
Nell'ipotesi che la dilatazione del mercurio sia lineare, cioč esprimibile tramite l'equazione l = a + b t, le costanti a e b vengono determinate in termini della lunghezza del tratto di mercurio alle temperature di riferimento di fusione del ghiaccio e di ebollizione dell'acqua a pressione atmosferica. Queste temperature vengono denominate rispettivamente di 0 e 100 gradi (Fig. 3).
Fig. 3
Sostituendo i valori di a e b nell'equazione termometrica, si ottiene la relazione che consente di determinare la generica temperatura t corrispondente al tratto di mercurio di lunghezza l . La suddivisione in 100 parti del tratto di mercurio compreso fra la lunghezza l0 e la lunghezza l100 permette di stabilire l'unitŕ di temperatura, detta grado centesimale o Celsius.
|
|
Inconvenienti delle scale empiriche
In
generale due termometri basati su fenomeni diversi, non segnano lo stesso valore
di temperatura, ad eccezione che per i punti fissi scelti convenzionalmente. Questo
perchč le equazioni termometriche delle sostanze sensibili alla temperatura sono
funzioni non lineari le cui costanti, a, b, c,..sono diverse da sostanza a sostanza.
Consideriamo ad esempio due scale termometrica basate su due diverse proprietŕ
termometriche: la dilatazione di un regolo di Cu e quella di uno regolo di Al.
Fissate le temperature di riferimento
a 0 °C e a 100 °C,
generalmente si ha che, a paritŕ di temperatura, le letture riportate dai due
termometri differiscono tra loro. La figura 4 mostra un andamento tipico dello
scarto fra le due letture.
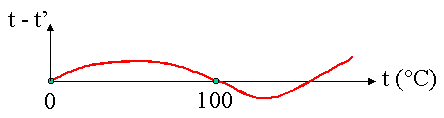
Fig. 4 t
- t’ = scarto delle indicazioni dei due termometri
Termometri a scala assoluta: termometri a gas
E'
possibile realizzare termometri indipendenti, entro certi limiti, dalle proprietŕ
della sostanza termodinamica.
L'equazione caratteristica di un gas in condizioni
di basse pressioni č: P
·V = n R t, dove
n, numero di moli, rappresenta la quantitŕ di gas, R č la costante universale
dei gas, t la temperatura del gas. Questa legge, che č la stessa indipendentemente
dal tipo di gas, viene detta anche equazione dei gas perfetti o ideali. Per una
fissata temperatura t, essa č rappresentata graficamente dal diagramma di Clapeyron
o da quello di Amagat.
| P ·V = cost Gas perfetto
|
P ·V = cost Gas perfetto
|
Nei limiti di validitŕ della legge dei gas perfetti, a paritŕ di volume V, c'č una diretta proporzionalitŕ fra pressione P e temperatura t. Il funzionamento dei termometri a gas si basa su su questa relazione. La Fig. 7 riporta il diagramma di Amagat per l'anidride carbonica a due temperature, 0 °C e 100 °C, per un ampio intervallo di pressioni.
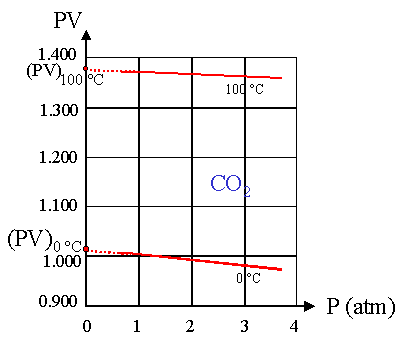 Fig.
7
Fig.
7
La pendenza diversa da zero e la non linearitŕ delle due curve evidenzia il discostarsi del gas dal comportamento, puramente ideale, di gas perfetto. Si verifica perň che, indicando con (PV)100 il limite per P tendente a zero (condizione di gas perfetto) del gas a 100°C e con (PV)0 lo stesso limite quando la temperatura del gas č di 0°C,
![]()
![]()
il rapporto (PV)100 / (PV)0 = 1.36610 ed č indipendente dal tipo di gas.
=cost.gif)
Tutto questo perchč a pressioni molto basse il comportamento del gas approssima la condizione di gas di gas ideale. Inoltre, indicando con
![]()
si ha che:

Di conseguenza, si puo concludere che:
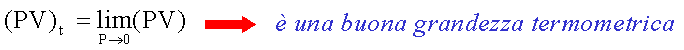
Č
possibile allora definire una scala termometrica assoluta, cioč una scala
indipendente dalla sostanza termometrica.
In una scala assoluta le temperature
si usa indicarle con le lettere maiuscole, per cui il rapporto tra le grandezze
termometriche diventa:
t.gif)
Una volta che si definisce convenzionalmente una temperatura di riferimento T’, la temperatura T si determina dalla relazione procedente misurando le grandezze termometriche (PV)T' e (PV)T.
|
| Fig.
8 Come temperatura
campione T' si č deciso di prendere la temperatura del punto triplo dell’acqua,
in cui si ha la coesistenza della fase solida, liquida e gassosa dell'acqua. Questa
scelta č conveniente perché al punto triplo la pressione č automaticamente determinata. Convenzionalmente: T' = Tpunto triplo= 273.16 K. L'unitŕ di temperatura viene indicata con la lettera maiuscola K priva del simbolo di grado e viene denominata grado Kelvin. |
La figura seguente mostra lo schema di principio di un termometro a gas. Il gas č in contatto termico con l'ambiente di cui si vuole misurare la temperatura, denominato termostato. Il volume del gas viene mantenuto fisso regolando la posizione verticale del serbatoio contenente del mercurio; questo serbatoio č collegato al serbatoio contenente il gas tramite un tubo flessibile. Il dislivello tra le superfici libere di mercurio, quella a contatto con il gas nel serbatoio A la cui quota viene mantenuta fissa, e quella a contatto con il vuoto, nel serbatoio B, č proporzionale alla pressione. Il dislivello č tanto minore quanto piů bassa č la temperatura del gas.
|
| Il gas contenuto in A ha massa m, pressione P, volume V e la stessa temperatura t del termostato. Equazione
di stato PV
= n R t |
Scala Celsius
La
temperatura di fusione del ghiaccio alla pressione atmosferica č uguale a 273.16
K. Per ottenere una scala centesimale, a partire da una scala assoluta, si esegue
una traslazione rispetto alla scala assoluta in modo che la temperatura di fusione
del ghiaccio sia uguale a 0 C°. Indicando con t la temperatura centesimale e T
quella in K, si ha che:
![]()
La scala termodinamica
Nel 1967 si decise di definire la temperatura basandosi sulla scala termodinamica. Poiché si dimostra anche che la scala termodinamica e quella assoluta sono identiche, non vi č ragione di distinguerle.