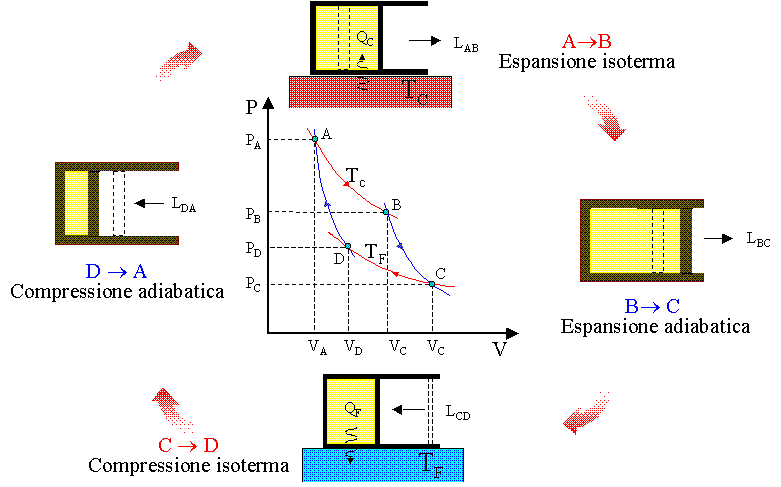
Ciclo di Carnot per un gas ideale
Ciclo reversibile composto da: due isoterme + due adiabatiche

 |
A®
B Espansione
isoterma, Q - L = D
U; gas
ideale ®
D
U=0, Q = L
B® C Espansione adiabatica, Q - L = D U, Q = 0, ® L = -D U,
C® D Compressione isoterma, Q = L
B® C Compressione adiabatica, L = -D U,
|
| Gli stati B e C sono sulla stessa adiabatica | 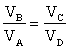 |
||
| Gli stati D e A sono sulla stessa adiabatica |
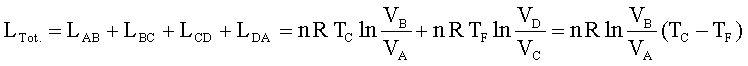
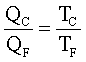
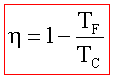
Considerazioni sul ciclo di Carnot
 |
|
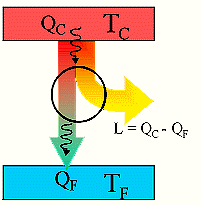
La potenza motrice del calore è indipendente dagli agenti impiegati per realizzarla; la sua quantità è fissata unicamente dalle temperature dei corpi fra i quali si effettua in definitiva il trasporto calorico (S. Carnot ).
L = QC - QF
|
|
La
potenza motrice di una cascata d’acqua dipende dalla sua altezza e
dalla quantità di liquido; la potenza motrice del calore dipende anch’essa
dalla quantità di calorico impiegate e da ciò che si potrebbe chiamare,
da ciò che in effetti chiameremo, l’altezza della caduta, cioè dalla
differenza di temperatura tra i corpi tra i quali si compie lo scambio del
calorico.
(S. Carnot ). |
Carnot, quando scrisse le sue Riflessioni, credeva che il calore fosse un fluido indistruttibile (calorico). In una macchina termica, la quantità di calore che fluisce dalla sorgente calda era considerata perciò uguale a quella che defluisce dalla sorgente fredda, così come la quantità di acqua in ingresso in una turbina ad acqua, alimentata da una cascata, è uguale a quella in uscita. Secondo questo modello la macchina di Carnot verrebbe rappresentata da un diagramma di flusso con i due tubi di flusso di QC e QF dello stesso diametro. Il lavoro si immaginava fosse estratto dal flusso discendente di calore così come, nella ruota ad acqua esso viene prodotto, sfruttando la differenza di energia potenziale dell’acqua. Nonostante questa immagine erronea sulla natura del calore Carnot determinò correttamente l’efficienza della sua macchina termica.
Importanza del Ciclo di Carnot
Il ciclo di Carnot è di notevole importanza per la Termodinamica, sia sotto l'aspetto applicativo che teorico. Dal punto di vista applicativo esso stabilisce un limite superiore al rendimento di una macchina termica, note la temperatura massima e minima del fluido di lavoro. Dal punto di vista teorico esso suggerisce la possibilità di definire una scala assoluta di temperatura e una nuova grandezza termodinamica, l'entropia. Parafrasando il titolo di una canzone di musica leggera, il ciclo di Carnot, ideale ma ricco di implicazioni, si potrebbe definirlo Bello e Impossibile!
Ragioni dell'importanza del ciclo di Carnot.
|
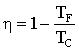 |
Il rendimento del ciclo di Carnot dipende dalle temperature delle riserve termiche ed è indipendente dalla sostanza termodinamica. Più grande è il gradiente termico delle riserve di calore e maggiore è il rendimento. |
|
|
|
|
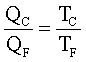 |
Il rapporto fra i calori che fluiscono nelle due riserve di calore dipende esclusivamente dal rapporto fra le temperature delle riserve. In particolare esso è indipendente dalla sostanza termodinamica soggetta al ciclo. Questo fatto suggerì a lord Kelvin l'idea di una scala assoluta di temperatura: la scala termodinamica della temperatura, o scala Kelvin. | ||
|
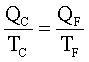 |
Il rapporto fra il flusso di calore e la temperatura della riserva termica in cui tale flusso ha luogo si conserva. Si osservi che la grandezza Q/T di una macchina reversibile si conserva: quella della sorgente calda è uguale a quella della sorgente fredda. Inoltre, la Q/T dell'universo è nulla, dato che QC/TC - QF/TF =0. La quantità Q/T della macchina diCarnot, probabilmente suggerì a Clausius il concetto di entropia. |
Cicli di Carnot per miscele liquido-vapore